外泌体样本的ELISA实验怎么做?
发布时间:2021-08-22 20:33:14来源:
外泌体(exosomes)是细胞分泌的微小囊泡,直径约30-100nm,存在于大多数体液(如血液、尿液和脊髓液)和细胞培养液当中。近年来,科研工作者在阐明外泌体的生理、病理生理功能及针对这些功能的临床应用方面开展了大量研究,尤其是疾病的诊断、治疗应用(如生物标志物的开发)方面。研究表明,肿瘤细胞的外泌体会释放与血管生成和免疫逃逸相关的分子标志物,说明外泌体可能与肿瘤细胞微环境的创建和促肿瘤生长有关1。此外,外泌体表面黏附分子的表达谱决定了肿瘤细胞转移的终点2。可见外泌体在肿瘤的发生发展中有着重要的研究价值。
在外泌体课题研究中,定量分析自然是必不可少的一步。ELISA是一种较为简单的检测样本中特定蛋白或细胞因子含量的方法。常见的ELISA检测样本有血清、血浆、组织、细胞上清等,那么外泌体样本的ELISA(以下均简称exo-ELISA)如何检测?应用场景是什么?其原理是什么?与普通ELISA技术相比,exo-ELISA检测有哪些不同?让我们一起来看看。
一、双抗体夹心法
将已知的外泌体表面分子(如CD9、CD63、CD81)作为标志物,事先将特定外泌体分子标志物的一抗包被于板底。当加入一定浓度的含外泌体的样本时,一抗就可以识别外泌体表面分子,实现捕获外泌体的目的。e.g.常用的ExoELISA-ULTRA外泌体定量分析检测试剂盒具有超高的灵敏度。
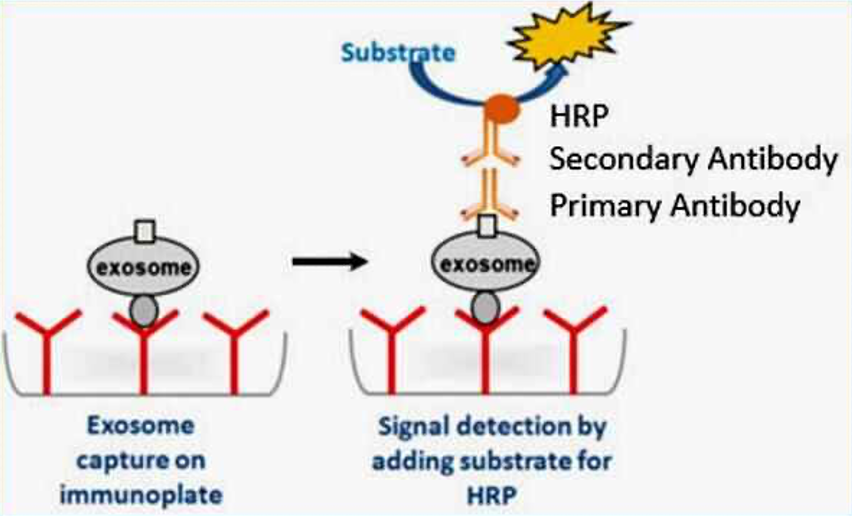
图1. 双抗体夹心法检测exosomes原理示意图
二、磷脂酰丝氨酸(phosphatidylserine,PS)亲和技术
已知Tim4(T细胞免疫球蛋白域和含粘蛋白域的蛋白4)可以通过位于细胞外区域的IgV结构域与PS结合,并具有钙离子依赖性3。而在螯合剂的作用之下,钙离子与螯合剂的配位原子相结合,致使Tim4与PS分离开来。
与双抗体夹心法不同的是,PS亲和技术检测exo-ELISA是使用磷脂酰丝氨酸事先包被的微孔板、生物素化的CD9、CD63、CD81一抗、亲和素标记的辣根过氧化物酶,借助于抗原-抗体反应、生物素-亲和素的结合反应来检测待测样本中外泌体含量的一种方法。与外泌体表面标记的特异性抗体相比,Tim4能够高效地捕获来自多种细胞类型的外泌体。这种方法也适用于外泌体的纯化。
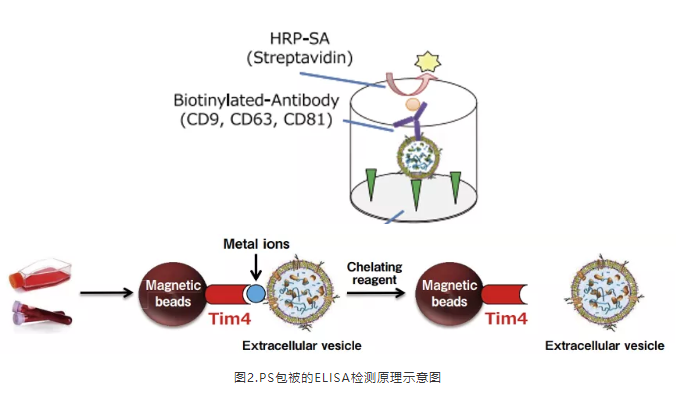
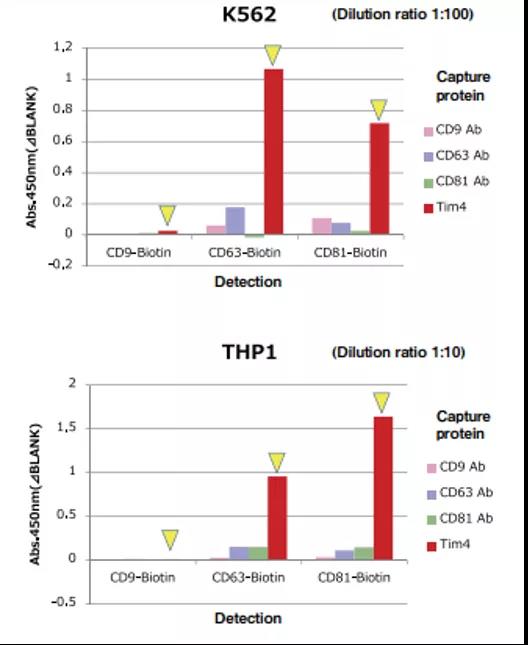
图3. 不同种类包被蛋白的检测灵敏度对比
三、磁珠法
磁珠法的基本原理是采用生物素标记的外泌体,亲和素标记的磁珠,利用生物素-亲和素的结合反应来对低外泌体含量的样本(如尿液、细胞上清)进行纯化。
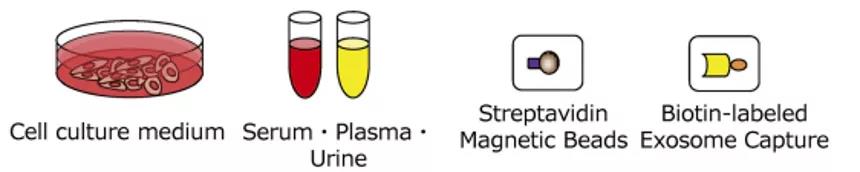
图4. 磁珠法纯化外泌体
四、基因工程的方法
DARPins是人工合成的由两个α-螺旋和一个β-转角的重复结构组成的合成肽,被设计为受体蛋白等多种靶点(如:Her2)的结合域。DARPin -G3表达于慢病毒衣壳或细菌表面,被报道可用于肿瘤的靶向治疗,是具有潜力的、可以克服单克隆抗体局限性的蛋白类治疗因子。
Khodashenas等4用重组LAMP-DARPins包装的慢病毒感染HEK293T细胞,使得外泌体表面表达重组嵌合蛋白。通过ELISA检测外泌体表面重组抗原的表达,来表征外泌体的含量。DARPins-G3是专门针对表皮生长因子Her2设计而成的,因此可以用于检测Her2+的SKBR3细胞外泌体的含量(图5)。该方法用于外泌体的捕获和纯化过程。
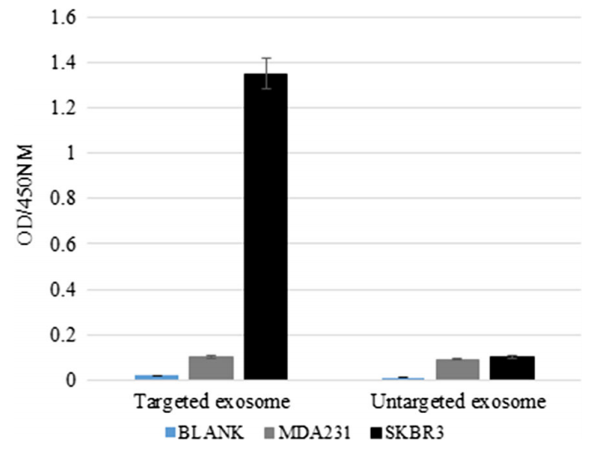
图5. 外泌体表达的DARPins与细胞表面Her2分子之间的反应
注:用MDA231细胞作为Her2阴性对照细胞,SKBR3为Her2阳性细胞。
五、PD-L1液体活检新方法的开发
研究表明,循环外泌体PD-L1水平可以区分肿瘤的存在,并与免疫治疗的反应有很好的相关性。2020年1月由杨朝勇教授4等开发的用于肿瘤液体活检的外泌体PD-L1 ELISA检测方法,通过筛选获得的PD-L1核酸适配体,结合微量热泳动效应,在较少的样本体积、均质性差的体液条件下,能够获得均质、高效、高灵敏度的检测结果。
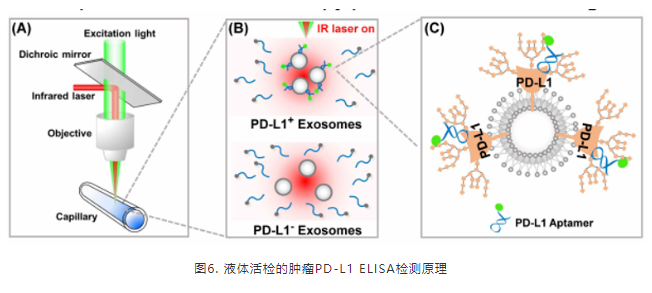
筛选过程中发现,MJ5对癌细胞表面PD-L1的结合效果最好,且对PD-L1阴性细胞无明显的结合。MJ5适配体经进一步优化得到由33个核苷酸组成的、发夹结构的MJ5C。
流式细胞术分析显示,PD-L1阳性细胞MJ5C核酸适配体的荧光强度高于对照序列,PD-L1阴性细胞未见明显的荧光增强(图7A-B)。
结合亲和力是指单个生物分子(如蛋白质或DNA)与其配体(如药物)之间相互结合的强度,通常通过平衡解离常数 (Kd) 来衡量。Kd值越小代表配体与蛋白质的亲和力越大。结合亲和力分析显示:PD-L1阳性细胞MJ5C核酸适配体与对照核酸适配体的荧光强度比不仅远高于已报道的真核细胞选择PD-L1蛋白的PD-L1适配体,而且比对照抗体的荧光强度比高约3倍(图7C)。这些结果表明,MJ5C适配体不仅具有良好的选择性,而且相比于PD-L1抗体组,它与PD-L1的结合效率更高。这种结合效率的提高可能是因为PD-L1的空间位阻效应,而MJ5C核酸适配体比PD-L1抗体小,因此较容易地避免了糖基化所产生的空间位阻效应。
为了证明这一假设,首先用肽-N-糖苷酶F (PNGase F)处理细胞,以在被适配体或PD-L1抗体染色前削减总N-连接糖基化水平。适配体染色的2组(糖基化/去糖基化组)之间荧光强度无明显变化;而与未处理相比,PNGase F处理后PD-L1阳性(HCT116)细胞的抗体染色荧光强度增强(图7D-E)。这些结果表明PD-L1的糖基化阻碍了PD-L1抗体对其的识别,而PD-L1适配体MJ5C受空间位阻的影响较小,很可能是由于其体积减小了10倍。因此,与PD-L1抗体相比,MJ5C适配体具有更高的分子识别能力,可以显著提高外泌体PD-L1检测的敏感性。
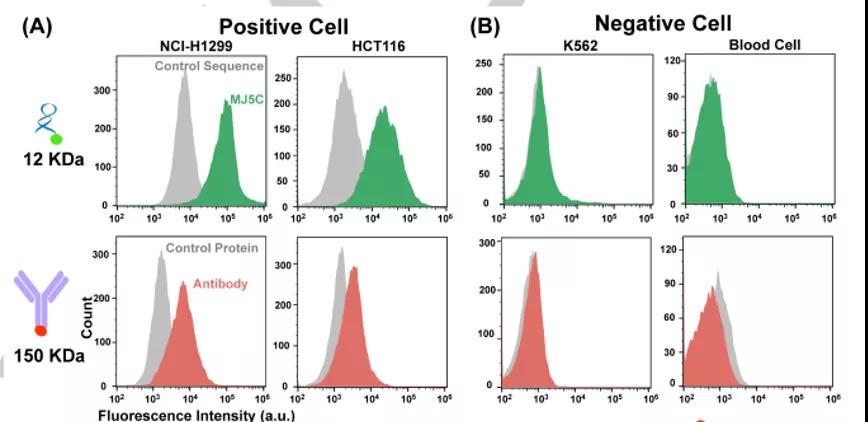
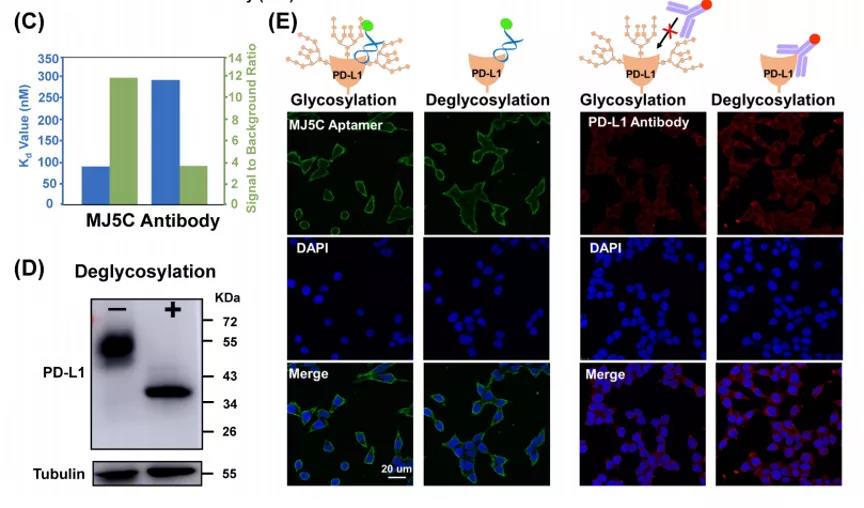
图7. MJ5C适配体与PD-L1抗体的结合性能比较
以上方法多是基于外泌体表面蛋白的检测,那么研究某个蛋白分子A在外泌体中表达的基本逻辑思路是怎样的呢?
首先,确定目的蛋白是位于外泌体囊泡内还是囊泡表面。
如果目的蛋白位于囊泡表面,通过流式细胞术检测即可,不需要透膜剂处理。具体方法为通过磁珠包被的IgA或者IgG进行捕获,采用CD81/CD63/CD9等作为一抗进行检测。
如果目的蛋白位于囊泡内部,则需要将分离得到的外泌体囊泡做破膜处理,类似于细胞破膜处理。即用含SDS的RIPA裂解液提取蛋白,然后进行ELISA检测。
所谓“细节决定成败”,希望大家在实验过程中多思考,抓住细节,多发高分文章!
【参考文献】
1. Tkach, M., & Théry, C. (2016). Communication by Extracellular Vesicles: Where We Are and Where We Need to Go. Cell, 164(6), 1226–1232.
2. Hoshino, A., Costa-Silva, B., Shen, T. L., Rodrigues, G., Hashimoto, A., Tesic Mark, M., Molina, H., Kohsaka, S., Di Giannatale, A., Ceder, S., Singh, S., Williams, C., Soplop, N., Uryu, K., Pharmer, L., King, T., Bojmar, L., Davies, A. E., Ararso, Y., Zhang, T., … Lyden, D. (2015). Tumour exosome integrins determine organotropic metastasis. Nature, 527(7578), 329–335.
3. Miyanishi, M., Tada, K., Koike, M., Uchiyama, Y., Kitamura, T., & Nagata, S. (2007). Identification of Tim4 as a phosphatidylserine receptor. Nature, 450(7168), 435–439.
4. Huang, M., Yang, J., Wang, T., Song, J., Xia, J., Wu, L., Wang, W., Wu, Q., Zhu, Z., Song, Y., & Yang, C. (2020). Homogeneous, Low-volume, Efficient, and Sensitive Quantitation of Circulating Exosomal PD-L1 for Cancer Diagnosis and Immunotherapy Response Prediction. Angewandte Chemie (International ed. in English), 59(12), 4800–4805.
说明:本内容由发布者创建和发布,如涉侵权,请联系发布者处理。本内容仅代表发布者观点,不代表平台立场。
相关推荐:
- 腹泻性贝类毒素(DSP)酶联免疫分析盒 腹泻性贝类毒素ELISA试剂盒
- 麻痹性贝类毒素ELISA试剂盒 麻痹性贝类毒素酶联免疫分析试剂盒
- 微囊藻毒素LR酶联免疫试剂盒 微囊藻毒素ELISA试剂盒
- 大豆球蛋白ELISA试剂盒 大豆球蛋白酶联免疫分析试剂盒
- β-伴大豆球蛋白ELISA试剂盒 β-伴大豆球蛋白酶联免疫试剂盒
- 大豆凝集素ELISA试剂盒 大豆凝集素(SBA)酶联免疫分析试剂盒
- 口蹄疫A型(AF72株)抗原检测ELISA试剂盒 口蹄疫A型(AF72株)抗原检测试剂盒
- 亚洲口蹄疫1型(JSL/06)抗原检测ELISA试剂盒 亚洲口蹄疫1型(JSL/06)抗原检测酶联免疫试剂盒
- 甲型口蹄疫(武汉株)抗原检测ELISA试剂盒甲型口蹄疫(武汉株)抗原
- 猪伪狂犬gB抗体检测试剂盒 猪伪狂犬gB抗体ELISA试剂盒 PRV GB试剂盒



